Hidrojen soygaz mıdır yoksa ametal midir?
Periyodik tabloda hidrojenin sınıflandırılması, kimyasal özelliklerinin çeşitliliği nedeniyle merak konusu olmuştur. Bu elementin elektron alma eğilimi, moleküler yapısı ve bileşik oluşturma davranışları, onu ametal grubuna yerleştiren belirleyici özelliklerdir.
Hidrojenin Sınıflandırması: Soygaz mı, Ametal mi?Hidrojen, periyodik tabloda benzersiz bir konuma sahip olan ve bu nedenle sınıflandırması sıkça tartışılan bir elementtir. Kısaca cevap vermek gerekirse:Hidrojen bir ametaldir, soygaz değildir. Ancak bu durumun detaylı açıklaması aşağıdaki gibidir: 1. Hidrojen Neden Ametal Olarak Sınıflandırılır?Hidrojen, kimyasal özellikleri bakımından ametallere benzer davranışlar sergiler:
2. Hidrojen Neden Soygaz Değildir?Soygazlar (asal gazlar), periyodik tablonun 8A grubunda yer alan ve kararlı elektron konfigürasyonları nedeniyle genellikle tepkimeye girmeyen elementlerdir. Hidrojenin soygazlardan farklı olduğu noktalar şunlardır:
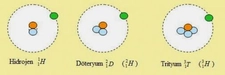
3. Hidrojenin Benzersiz Özellikleri ve Karışıklığın Nedeni Hidrojenin sınıflandırmasının kafa karıştırıcı olmasının nedeni, bazı özelliklerinin farklı grupları anımsatmasıdır:
Sonuç Hidrojen, kimyasal davranışları ve elektron yapısı göz önüne alındığında net bir şekilde ametal olarak sınıflandırılır. Ancak periyodik tablodaki konumu ve bazı özellikleri nedeniyle alkali metaller, halojenler ve soygazlarla kısmi benzerlikler gösterebilir. Bu benzersiz karakteri, onu periyodik tablonun en sıra dışı elementlerinden biri yapar. |













.webp)